Leghe di Zinco da Pressofusione
Interazione con l’Ambiente
Resistenza alla Corrosione
Lo zinco ha un’ottima resistenza alla corrosione in molti ambienti, e questo ha incrementato notevolmente il suo utilizzo per la protezione contro la corrosione. Nella maggior parte dei casi, il comportamento delle leghe di zinco pressocolate è simile a quello dello zinco non legato: i getti di zinco pressocolati si comportano bene in tutte quelle applicazioni dove lo zinco o l’acciaio galvanizzato sono ritenuti idonei; l’eccezione è rappresentata dai severi ambienti marini. La tabella 1 mette a confronto le velocità di corrosione dello zinco ad elevata purezza e dei pressocolati di zinco in diversi ambienti. La lega di zinco pressocolata, come le altre forme dello zinco, si corrode generalmente ad una velocità ridotta e costante; i getti che soddisfano i requisiti della EN 12844 (ed altre specifiche simili nel resto del mondo) non sono soggetti alla corrosione intercristallina. Questa forma di corrosione, che può condurre ad un rapido cedimento, si può verificare soltanto quando impurità dannose (in special modo stagno e piombo) superano i livelli specificati. Nella maggior parte dei paesi si seguono dei controlli che garantiscono il mantenimento di un severo controllo analitico sulla lega, cosicché le impurità non raggiungano mai tali livelli.
La letteratura riguardante la resistenza alla corrosione dello zinco in tutte le sue forme è vastissima. E’ stata recensita nella monografia “Zinc: Its Corrosion Resistance” (riferimento 11), alla quale si dovrebbe fare riferimento per ottenere informazioni più dettagliate rispetto a quelle contenute nel presente manuale.
Corrosione in Atmosfera
I pressocolati di zinco, quando lasciati esposti all’atmosfera ambientale, perdono presto il loro aspetto metallico brillante: esso è sostituito da un rivestimento compatto ed aderente di prodotti da corrosione, il quale protegge il componente da un ulteriore attacco.
La tabella sottostante mostra le velocità di corrosione che è possibile riscontrare nei pressocolati di zinco; è difficile che i valori possano superare i 12μm/anno, così com’è difficile che possano essere inferiori ad un decimo di questo valore. In Europa, negli ultimi anni, la riduzione dei livelli di SO2 nell’atmosfera ha portato verso una marcata diminuzione per ciò che concerne il tasso di corrosione, sia negli ambienti urbani che in molti ambienti industriali. I tassi relativi agli ambienti industriali mostrati in tabella possono essere significativamente più elevati rispetto a quelli che ci si può aspettare oggi in pratica.
Un rivestimento protettivo è richiesto unicamente là dove si prevede d’incontrare i tassi di corrosione più elevati, ovvero in severi ambienti industriali e marini.
Tassi di Corrosione dello Zinco e delle Leghe di Zinco in Diverse Atmosfere
|
Materiale
|
Sito
|
Tipo d’atmosfera
|
Corrosionemicron/anno
|
|
Zinco ad elevata purezza
|
Khartoum. Sudan
|
secca tropicale
|
0.25
|
|
Zinco ad elevata purezza
|
Abisto. Svezia
|
sub polare
|
0.25
|
|
Zinco ad elevata purezza
|
Cardington, Bedfordshire. Regno Unito
|
rurale
|
3.00
|
|
Zinco ad elevata purezza
|
State College, Pennsylvania. USA
|
rurale
|
1.00
|
|
Zinco ad elevata purezza
|
Wakefield, Yorkshire. Regno Unito
|
industriale
|
6.00
|
|
Zinco ad elevata purezza
|
New York. USA
|
industriale
|
7.00
|
|
Lega di zinco pressocolata
|
New York. USA
|
industriale
|
6.00
|
|
Zinco ad elevata purezza
|
Euston, London. Regno Unito
|
industriale
|
10.00
|
|
Zinco ad elevata purezza
|
Key West, Florida. USA
|
marino
|
3.00
|
|
Lega di zinco pressocolata
|
Key West, Florida. USA
|
marino
|
10.00
|
|
Zinco ad elevata purezza
|
Montauk Point, Long Island. USA
|
marino
|
3.00
|
|
Lega di zinco pressocolata
|
Montauk Point, Long Island. USA
|
marino
|
10.00
|
In qualsiasi condizione ambientale (interna od esterna) dove la condensa abbia la possibilità di formarsi sulla superficie e di rimanervi per lunghi periodi, si assiste alla formazione di un evidente prodotto bianco da corrosione, del tutto simile alla “ruggine bianca” che si genera sulle superfici galvanizzate in condizioni simili. Questa forma di corrosione di solito non causa una perdita molto rapida di metallo, ma deve essere comunque prevenuta per ragioni estetiche: un ricoprimento chimico può fornire un’adeguata protezione. Questo tipo di protezione è raccomandato quando i getti pressocolati devono essere trasportati od utilizzati in ambienti tropicali senza essere protetti, oppure impiegati all’esterno in ambienti costieri.
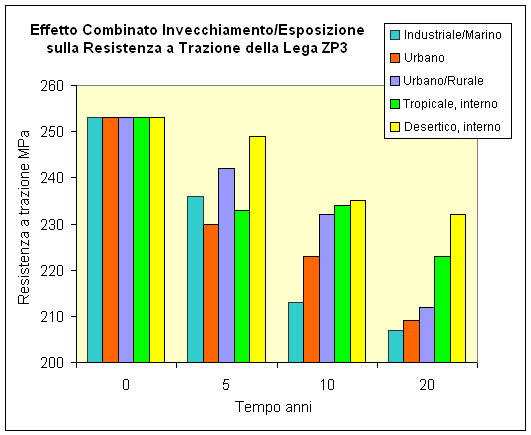
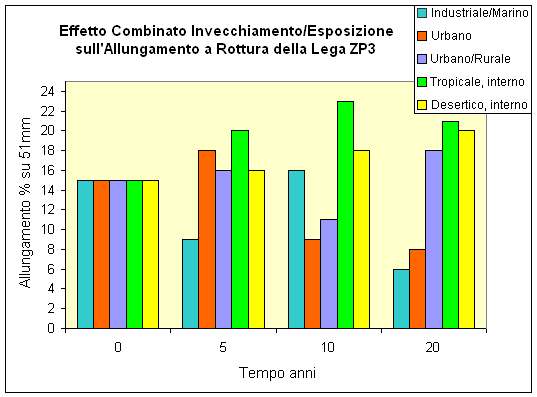
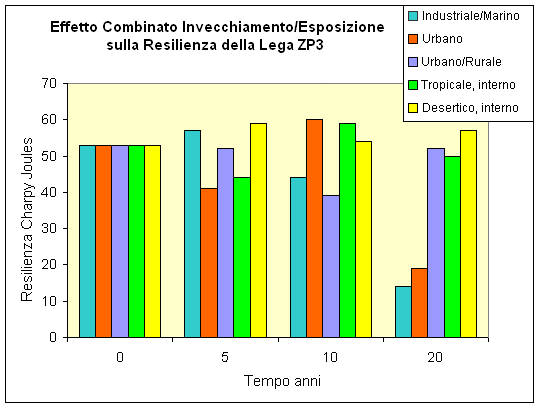
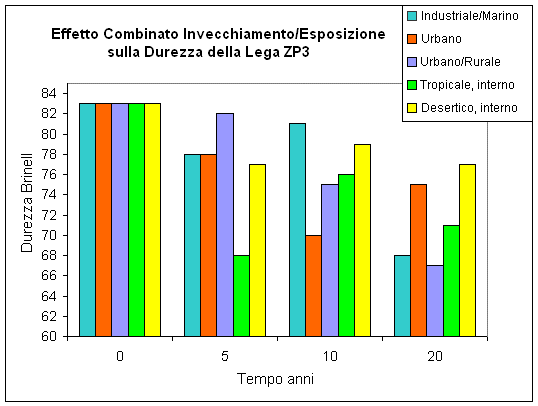
Dato che l’effetto della corrosione sulle proprietà meccaniche è spesso importante, la tabella sottostante riassume i cambiamenti delle proprietà meccaniche durante un’esposizione di 20 anni in diversi siti; essa fornisce una testimonianza rilevante sulla durata dei pressocolati di zinco.
Effetto Combinato dell’Esposizione e dell’Invecchiamento sulle Proprietà Meccaniche della Lega di Zinco Pressocolata (ASTM AG 4OA, equivalente alla ZP3).
|
New York.
NY (esterno) Industriale/ Marino |
Altoona,
Pennsylvania (esterno) Urbano |
State College.
Pennsylvania (esterno) Urbano/Rurale |
Coco Solo Islands.
Canal Zone (interno) Tropicale |
Tucson.
Arizona (interno) Desertico |
|
|
Resistenza a Trazione MPa
|
|||||
|
Originale
|
253
|
253
|
252
|
253
|
253
|
|
Cinque anni
|
236
|
230
|
242
|
233
|
249
|
|
Dieci anni
|
213
|
223
|
232
|
234
|
235
|
|
Venti anni
|
207
|
209
|
212
|
223
|
232
|
|
Allungamento % on 50.8mm
|
|||||
|
Originale
|
15
|
15
|
15
|
15
|
15
|
|
Cinque anni
|
9
|
18
|
16
|
20
|
16
|
|
Dieci anni
|
16
|
9
|
11
|
23
|
18
|
|
Venti anni
|
6
|
8
|
18
|
21
|
20
|
|
Durezza (Rockwell E)
|
|||||
|
Originale
|
83
|
83
|
83
|
83
|
83
|
|
Cinque anni
|
78
|
78
|
82
|
68
|
77
|
|
Dieci anni
|
81
|
70
|
75
|
76
|
79
|
|
Venti anni
|
68
|
75
|
67
|
71
|
77
|
|
Resilienza (Charpy) J
|
|||||
|
Originale
|
53
|
53
|
53
|
53
|
53
|
|
Cinque anni
|
57
|
41
|
52
|
44
|
59
|
|
Dieci anni
|
44
|
60
|
39
|
59
|
54
|
|
Venti anni
|
14
|
19
|
52
|
50
|
57
|
|
Cambiamento dimensionale%
|
|||||
|
Cinque anni
|
-0.01
|
-0.01
|
-0.01
|
-0.01
|
-0.01
|
|
Dieci anni
|
-0.02
|
-0.01
|
0.00
|
0.00
|
-0.01
|
|
Venti anni
|
-0.02
|
-0.02
|
0.00
|
0.00
|
-0.01
|
Le cifre riportate nella tabella superiore sono rappresentate nei grafici di seguito:
Finiture Superficiali dei Pressocolati
Nel caso in cui i getti debbano essere impiegati per lunghi periodi in ambienti aggressivi, oppure l’aspetto grigio opaco dello zinco esposto alle intemperie non sia accettabile, i pressocolati di zinco sono spesso sottoposti ad una notevole varietà di differenti processi di finitura.
Frequentemente si fa ricorso al rivestimento con vernici liquide o a polvere: è opportuno ricordare che in questi casi le ricoperture organiche sullo zinco hanno una durata superiore rispetto alla loro applicazione sul ferro e sull’acciaio. Se nel normale corso degli eventi lo strato di vernice si crepa oppure si sviluppano delle porosità (probabilmente come risultato dell’azione degli agenti atmosferici), allora il cedimento completo che ne consegue, nel caso di materiali come il ferro e gli acciai, avviene molto rapidamente: la corrosione si estende lungo l’interfaccia tra l’acciaio e la ricopertura, provocando il sollevamento di ampie porzioni di materiale in modo piuttosto rapido. Sullo zinco, invece, la corrosione non si sviluppa lungo l’interfaccia, e pertanto la vita effettiva del rivestimento è maggiore.
Spesso i pressocolati in lega di zinco sono anche cromati. Nel caso in cui sia adottata questa finitura, per fornire almeno in parte una protezione contro la corrosione, è importante che siano applicati, preventivamente, degli spessori di rame e nichel sufficienti per le condizioni di servizio previste (vedere la normativa EN 12540:2000). .
Corrosione in Gas Diversi dall’Aria
L’ossigeno, l’azoto, il biossido di carbonio, i gas di scarico e quelli inerti non corrodono lo zinco, ma se è presente dell’umidità è possibile che si formino delle “macchie da stoccaggio umido”. Nel caso in cui sia necessario evitare questo fenomeno, i getti dovrebbero essere passivati. I pressocolati di zinco sono adottati per alcuni componenti nella fornitura del gas naturale (per esempio i regolatori di gas) e sono stati utilizzati per molti anni nei componenti delle apparecchiature per lo stoccaggio dei gas.
Contatto con Acqua Dolce
In alcune parti del mondo i pressocolati di zinco sono utilizzati con successo nella raccorderia per l’acqua, ma il tasso di corrosione dello zinco nell’approvvigionamento delle acque dolci varia molto secondo la durezza, la composizione chimica e l’acidità dell’acqua. I tassi variano in modo considerevole, ma i valori sono generalmente compresi tra 2,5μm e 100μm l’anno. Le acque dure provocano in genere una corrosione inferiore, perché l’incrostazione di carbonato di calcio che si deposita in superficie riduce il tasso d’attacco. Anche l’origine dell’acqua può avere un effetto importante, in modo particolare sui tassi di corrosione in acqua calda: poiché le acque delle sorgenti superficiali contengono minuscole quantità di composti organici, esse favoriscono il depositarsi dell’incrostazione in forma molto aderente (quasi come il guscio di un uovo) con un effetto protettivo massimo. Le acque provenienti da pozzi profondi provocano in genere il depositarsi di un’incrostazione irregolare e meno aderente, la quale fornisce allo zinco una protezione molto inferiore. Il pH della maggior parte delle acque potabili è compreso tra 5.0 e 8.5; la corrosione dello zinco di solito è più bassa per valori compresi tra 6.5 e 12. Nel caso in cui sia previsto l’utilizzo di pressocolati di zinco a contatto continuo con le acque d’approvvigionamento, si dovrebbe eseguire un’indagine approfondita per verificare se questi possono dare buone prestazioni senza rivestimenti protettivi. Oltre a questi fattori ne esistono altri importanti, come ad esempio l’anidride carbonica libera: i tassi di attacco più elevati sono determinati dalle acque con un elevato contenuto di anidride un residuo fisso molto basso.
Contatto con Acqua Marina
L’esperienza nell’utilizzo dei pressocolati di zinco in acqua salata non è ampia, ma le conoscenze derivanti dalle altre forme dello zinco suggeriscono che per le condizioni di totale immersione ci si può aspettare un tasso di corrosione compreso tra 12μm e 25μm l’anno. I tassi di corrosione aumentano in modo abbastanza considerevole quando l’immersione è intermittente, come nella zona di marea: mentre il tasso di corrosione nel caso d’immersione totale può essere tollerato, nel caso d’alcune applicazioni, con getti sottoposti ad immersioni alternate, è necessario ricorrere ad una protezione adeguata. La corrosione è inoltre accelerata dal contatto con altri metalli.
Contatto con Altre Soluzioni Acquose
Come regola generale, i pressocolati di zinco dovrebbero essere utilizzati soltanto a contatto con soluzioni dal pH compreso tra 6.5 e 12, dato che il tasso di corrosione cresce rapidamente al di fuori di questi estremi. Esistono comunque altri fattori come l’agitazione, la temperatura e la polarizzazione che possono essere importanti e che sono in grado di cambiare in modo significativo il tasso d’attacco rispetto a quello che potrebbe essere previsto altrimenti. I risultati dettagliati relativi a diverse soluzioni sono stati raccolti nel manuale “Zinc: Its Corrosion Resistance”. Diversamente, bisognerebbe eseguire dei test atti a verificare la compatibilità dei pressocolati nell’utilizzo con soluzioni acquose, detergenti e saponi. La maggior parte dei detergenti è alcalina, e per questa ragione hanno un tasso d’attacco piuttosto lento che risulta essere accettabile nella maggior parte dei casi. Le soluzioni detergenti concentrate o molto calde possono attaccare più rapidamente i getti di zinco non protetti
Contatto con Materiali Organici
Le sostanze organiche presentano in genere un impatto minimo sullo zinco, a meno che non sia presente dell’acqua unita ad un acido, in modo naturale oppure come risultato di prodotti usualmente presenti sotto forma d’emissioni atmosferiche. Il tricloroetilene (trielina), ad esempio, non reagisce con i pressocolati di zinco e così neppure l’alcol anidro, ma in entrambi i casi, se è presente dell’acqua, ci si può aspettare un aumento della corrosione. Gli oli raffinati non attaccano lo zinco, a meno che non contengano quantità apprezzabili di solfuri, acqua o composti acidi. Ad esempio, il petrolio contenente acqua può dar luogo a prodotti di corrosione che possono bloccare gli iniettori di carburante dei jet. E’ stato dimostrato che il trattamento di cromatura previene questo fenomeno, ma ad oggi i componenti in zinco del sistema di carburazione necessitano raramente di essere cromati. Anche il combustibile diesel, se contiene dei solfuri, può dar luogo a composti che bloccano l’apporto di carburante. I lubrificanti a base di prodotti animali dovrebbero essere impiegati con cautela, poiché contengono acidi formati dall’ossidazione, mentre quelli puramente minerali sono generalmente soddisfacenti. Nella monografia ‘“Zinc: Its Corrosion Resistance” sono riportati gli effetti di diverse sostanze.
Contatto con Cibi e Bevande
Le superfici dei getti di zinco appena colati non dovrebbero essere poste a contatto con i generi alimentari, a meno che non si sia certi che rimangono asciutte. Diversamente, lo zinco deve essere adeguatamente protetto mediante rivestimenti di rame-nichel-cromo o con altri rivestimenti impermeabilizzanti. La leggera acidità presente in molti alimenti può attaccare lo zinco e conferire al cibo uno spiacevole sapore metallico. Per la stessa ragione, anche i pressocolati di zinco impiegati in qualsiasi attrezzatura per contenere o conservare le bevande dovrebbero essere rivestiti od almeno protetti. Il consumo di cibo contaminato con lo zinco può provocare vomito, ma non è pericoloso: in ogni caso questo problema emerge raramente proprio a causa del cattivo sapore.
Corrosione per Contatto con Altri Metalli
Quando due metalli differenti sono posti a contatto in un ambiente corrosivo, essi formano una cella elettrolitica ed un flusso di corrente dal metallo base (anodo) verso il metallo nobile (catodo). Il risultato è che il tasso di corrosione dei metalli tende a diminuire per il metallo più nobile ed ad aumentare, a parità di condizioni ambientali, per il metallo meno nobile. La forza motrice per questa reazione elettrolitica è data dalla differenza di potenziale tra i metalli. Sebbene questa possa essere misurata in laboratorio (si veda la tabella delle serie elettrochimiche proposta di seguito), non è una guida affidabile per stimare la severità dell’aumento di corrosione derivante dal contatto bi-metallico. Questo fenomeno è alla base di un metodo utilizzato in alcune circostanze per proteggere l’acciaio (protezione catodica). Alcune parti in zinco opportunamente sagomate sono poste in contatto elettrico con l’acciaio che deve essere protetto (frequentemente strutture marine o condotte interrate): mentre l’acciaio é preservato, lo zinco è costantemente consumato. La corrosione bi-metallica dei pressocolati di zinco è raramente un problema. Diversi milioni di getti che sono in servizio hanno inserti in ottone, bronzo ed altri metalli nobili e non hanno mostrato alcun aumento apprezzabile del tasso di corrosione. In generale, è quindi ragionevole ipotizzare che sotto condizioni di corrosione atmosferica medie o moderatamente severe si verifichi un certo aumento della corrosione, anche se nella maggior parte dei casi è improbabile che questo aumento colpisca la funzionalità dei componenti. In condizioni d’immersione si dovrebbe evitare il contatto con il rame e le sue leghe.
Corrosione Aggiuntiva dello Zinco e delle Leghe Base di Zinco
Conseguente al Contatto con Altri Metalli o con il Carbonio
|
Metallo a contatto
|
Ambiente
|
||||
|
Atmosferico
|
Immerso
|
||||
|
Rurale
|
Industriale/urbano
|
Marino
|
Acqua dolce
|
Acqua salata
|
|
|
Alluminio e leghe d’alluminio
|
0
|
0 – 1
|
0 – 1
|
1
|
1 – 2
|
|
Bronzi all’alluminio e bronzi al silicio
|
0 – 1
|
1
|
1 – 2
|
1 – 2
|
2 – 3
|
|
Ottoni ad alta trazione, ottone (bronzo al manganese).
|
0 – 1
|
1
|
0 – 2
|
0 – 2
|
2 – 3
|
|
Cadmio
|
0
|
0
|
0
|
0
|
0
|
|
Carbonio
|
0 – 1
|
1
|
1 – 2
|
1 – 2
|
2 – 3
|
|
Ghise
|
0 – 1
|
1
|
1 – 2
|
1 – 2
|
2 – 3
|
|
Ghisa (austenitiche)
|
0 – 1
|
1
|
1 – 2
|
1 – 2
|
1 – 3
|
|
Cromo
|
0 – 1
|
1 – 2
|
1 – 2
|
1 – 2
|
2 – 3
|
|
Rame
|
0 – 1
|
1 – 2
|
1 – 2
|
1 – 2
|
2 – 3
|
|
Cupronichel
|
0 – 1
|
0 – 1
|
1 – 2
|
1 – 2
|
2 – 3
|
|
Oro
|
0 – 1
|
1 – 2
|
1 – 2
|
1 – 2
|
2 – 3
|
|
Bronzi allo zinco, bronzi al fosforo e bronzi allo stagno
|
0 – 1
|
1
|
1 – 2
|
1 – 2
|
2 – 3
|
|
Piombo
|
0
|
0 – 1
|
1 – 2
|
0 – 1
|
0 – 2
|
|
Magnesio leghe di magnesio
|
0
|
0
|
0
|
0
|
0
|
|
Nichel
|
0 – 1
|
1
|
1 – 2
|
1 – 2
|
2 – 3
|
|
Leghe nichel-rame
|
0 – 1
|
1
|
1 – 2
|
1 – 2
|
2 – 3
|
|
Leghe nichel-cromo-ferro
|
0 – 1
|
1
|
1 – 2
|
1 – 2
|
1 – 3
|
|
Leghe nichel-cromo-molibdeno
|
0 – 1
|
1
|
1 – 2
|
1 – 2
|
1 – 3
|
|
Argentana
|
0 – 1
|
1
|
1 – 2
|
1 – 2
|
1 – 3
|
|
Platino
|
0 – 1
|
1 – 2
|
1 – 2
|
1 – 2
|
2 – 3
|
|
Rodio
|
0 – 1
|
1 – 2
|
1 – 2
|
1 – 2
|
2 – 3
|
|
Argento
|
0 – 1
|
1 – 2
|
1 – 2
|
1 – 2
|
2 – 3
|
|
Leghe per saldare dure
|
0 – 1
|
1
|
1 – 2
|
1 – 2
|
2 – 3
|
|
Leghe per saldare dolci
|
0
|
0
|
0
|
0
|
0
|
|
Acciai inossidabili (austenitici ed altri tenori contenenti approssimativamente il 18% di cromo)
|
0 – 1
|
0 – 1
|
0 – 1
|
0 – 2
|
1 – 2
|
|
Acciai inossidabili (tenori martensitici
contenenti approssimativamente il 13% di cromo)
|
0 – 1
|
0 – 1
|
0 – 1
|
0 – 2
|
1 – 2
|
|
Acciai (al carbonio e debolmente legati)
|
0 – 1
|
1
|
1 – 2
|
1 – 2
|
1 – 2
|
|
Stagno
|
0
|
0 – 1
|
1
|
1
|
1 – 2
|
|
Titanio e leghe di titanio
|
0 – 1
|
1
|
1 – 2
|
0 – 2
|
1 – 3
|
|
Zinco e leghe base di zinco
|
0
|
0
|
0
|
0
|
0
|
Valori:
0. Le leghe base zinco presentano una corrosione nulla o comunque molto bassa e tollerabile in servizio.
1. Le leghe base zinco presentano una corrosione leggera o moderata, tollerabile in alcune circostanze.
2. Le leghe base zinco presentano una corrosione abbastanza severa, solitamente sono necessarie misure protettive.
3. Le leghe base zinco presentano una corrosione severa per cui si dovrebbe evitare il contatto.
Note generali: i valori tra parentesi sono basati su prove molto limitate, e sono perciò meno precisi rispetto agli altri valori mostrati. La tabella è in termini di corrosione addizionale ed il simbolo 0 non significa che i metalli a contatto non necessitano di protezione in tutte le condizioni di esposizione.
Serie e Potenziali Elettrochimici
|
Elemento
|
Reazione
|
Potenziale
di elettrodo
Volts
|
|
Oro
|
Au+ + e– = Au
|
1.692
|
|
Oro
|
Au3+ + 3 e– = Au
|
1.498
|
|
Platino
|
Pt2+ + 2 e– = Pt
|
1.18
|
|
Palladio
|
Pd2+ + 2 e– = Pd
|
0.951
|
|
Argento
|
Ag+ + e– = Ag
|
0.7996
|
|
Rame
|
Cu+ + e– = Cu
|
0.521
|
|
Rame
|
Cu2+ + 2 e– = Cu
|
0.3419
|
|
Ferro
|
Fe3+ + 3 e– = Fe
|
-0.037
|
|
Piombo
|
Pb2+ + 2 e– = Pb
|
-0.1262
|
|
Stagno
|
Sn2+ + 2 e– = Sn
|
-0.1375
|
|
Nichel
|
Ni2+ + 2 e– = Ni
|
-0.257
|
|
Cobalto
|
Co2+ + 2 e– = Co
|
-0.28
|
|
Cadmio
|
Cd2+ + 2 e– = Cd
|
-0.403
|
|
Ferro
|
Fe2+ + 2 e– = Fe
|
-0.447
|
|
Cromo
|
Cr3+ + 3 e– = Cr
|
-0.744
|
|
Zinco
|
Zn2+ + 2 e– = Zn
|
-0.7618
|
|
Cromo
|
Cr2+ + 2 e– = Cr
|
-0.913
|
|
Manganese
|
Mn2+ + 2 e– = Mn
|
-1.185
|
|
Titanio
|
Ti3+ + 3 e– = Ti
|
-1.37
|
|
Titanio
|
Ti2+ + 2 e– = Ti
|
-1.63
|
|
Alluminio
|
Al3+ + 3 e– = Al
|
-1.662
|
|
Magnesio
|
Mg2+ + 2 e– = Mg
|
-2.372
|
|
Magnesio
|
Mg+ + e– = Mg
|
-2.7
|
|
Sodio
|
Na+ + e– = Na
|
-2.71
|
|
Calcio
|
Ca2+ + 2 e– = Ca
|
-2.868
|
|
Potassio
|
K+ + e– = K
|
-2.931
|
|
Litio
|
Li3+ + e– = Li
|
-3.0401
|
|
Calcio
|
Ca+ + e– = Ca
|
-3.8
|
Tabella delle Differenze di Potenziale tra lo Zinco ed Altri Metalli Comuni
e Leghe in Soluzione Salina al 2%
|
Materiale
|
Composizione
|
Potenziale
millivolts
|
|
Platino
|
1400
|
|
|
Oro
|
1270
|
|
|
Acciaio inossidabile, passivo
|
18%Cr 8%Ni
|
1150
|
|
Cromo, passivo
|
1150
|
|
|
Argento
|
1050
|
|
|
Mercurio
|
1050
|
|
|
Nichel
|
970
|
|
|
Arcap
|
Cu55% Zn23% Ni 22%
|
950
|
|
Rame
|
830
|
|
|
Bronzo all’alluminio
|
Cu90% Al10%
|
800
|
|
Ottone
|
Cu Zn39%
|
750
|
|
Bronzo
|
Cu88% Sn12%
|
630
|
|
Stagno
|
600
|
|
|
Piombo
|
560
|
|
|
Acciaio dolce
|
0.08 – 0.12% C
|
400
|
|
Acciaio duro
|
0.8 – 1.2% C
|
305
|
|
Cadmio
|
300
|
|
|
Ferro
|
295
|
|
|
Metallo bianco
|
Sn 75% Zn25%
|
40
|
|
Zinco
|
0
|
|
|
Almasilium
|
Al 5% Mg
|
-295
|
|
Duralinox
|
Al Mg3% Al Mg5%
|
-300
|
|
Alluminio 99.5%
|
-310
|
|
|
Alpax H
|
Al Si 10% Mg
|
-335
|
|
Duralumin
|
Al Cu4% Mg
|
-530
|